
國自然熱點追蹤——線粒體代謝、線粒體功能障礙與胃腸道疾病的調控
瀏覽:147
發表時間:2025-06-27
目前已有大量研究指出線粒體在炎癥性腸病(IBD)和結直腸癌(CRC)中發揮關鍵作用,但線粒體功能障礙與這兩種疾病之間的因果關系尚不清楚。一些研究表明,炎癥反應和腸道微生物群可直接影響線粒體,導致其功能異常;然而,其他研究則顯示,即時在沒有發生炎癥的情況下,線粒體功能也可能受到影響。
其次,IBD或CRC治療的挑戰之一是不同患者之間的異質性,隨著組學的發展,提供了探索IBD和線粒體功能紊亂之間關系的工具,研究發現脂肪酸β-氧化(FAO)和丙酮酸代謝、氨基酸代謝和三羧酸循環(TCA)的代謝中間體在IBD患者發生改變。因此,需要深入探究腸道疾病中線粒體功能異常的分子機制,揭示胃腸道疾病代謝異質性規律,以推動線粒體靶向治療以及精準治療的臨床發展和優化。
研究要點
線粒體健康對于上皮屏障功能至關重要,包括細胞間連接、分泌的細胞外屏障(黏液和抗菌肽)以及誘導免疫耐受的共生微生物群。
線粒體產生的因子(線粒體活性氧和釋放的線粒體DNA)會造成組織損傷和病理反應持續。
參與線粒體功能和質量控制的基因突變與炎癥性腸病有關,炎癥性損傷導致炎癥性腸病的線粒體功能障礙。
腸上皮細胞線粒體功能障礙抑制氧化磷酸化、提高氧水平、破壞黏膜氧梯度,導致為宿主上皮供能的厭氧菌的損失。
線粒體功能障礙與細胞類型的改變有關,這些改變在慢性損傷的情況下會引起結直腸腫瘤的發生。在已確診的結直腸癌中,線粒體代謝促進了癌癥的生長。
線粒體靶向治療可以為基于基因突變、線粒體代謝或應激生物標志物的特定亞型患者提供雙重治療方法。
一、腸上皮細胞(IEC)的線粒體代謝、線粒體ROS(mtROS)和線粒體驅動的表觀遺傳調控
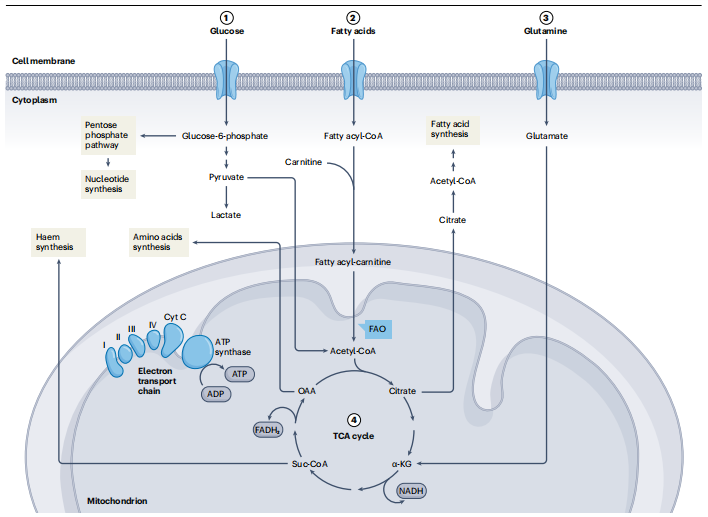
線粒體代謝在IEC中的作用:
線粒體是細胞能量代謝的核心,線粒體是通過氧化磷酸化(OxPHOS)產生ATP的場所。成熟的腸細胞和結腸細胞更依賴OxPHOS,這種依賴性導致高耗氧量,有助于管腔中的缺氧環境。這種“生理性上皮缺氧”有助于維持小鼠結腸中由專性厭氧細菌主導的腸道微生物群組成。
線粒體ROS信號傳導:
①低生理水平的mtROS,在激活各種反應以維持細胞穩態方面發揮著至關重要的作用。雖然ROS是生理信號傳導所必需的,但慢性升高的ROS在腸道炎癥期間是病理性的。
②線粒體質量控制機制的調控,包括裂變和融合、生物發生和線粒體自噬,均受mtROS動態調控。
線粒體代謝的表觀遺傳軸:線粒體通過提供必需的代謝產物,如乙酰輔酶A(acetyl-CoA)和S-腺苷甲硫氨酸(SAMe),對組蛋白乙酰化、組蛋白甲基化和 DNA 甲基化起到關鍵作用,進而影響基因表達和細胞功能。
二、上皮細胞線粒體功能障礙對炎癥性腸病(IBD)發生和發展的影響
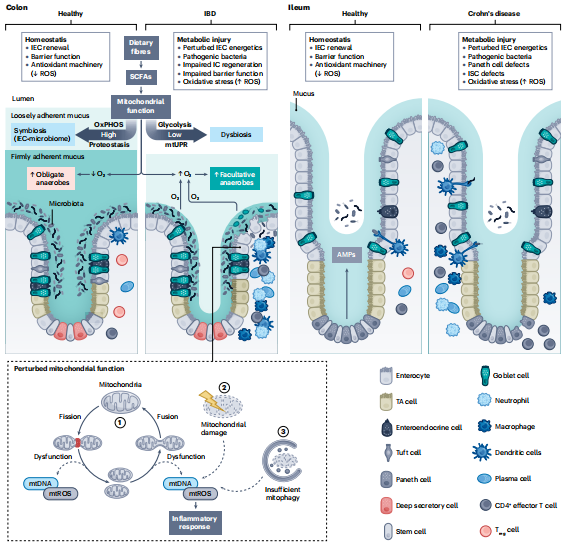
腸道炎癥導致線粒體功能障礙:
炎癥環境下,免疫細胞釋放的炎癥因子和ROS能夠直接損傷IEC的線粒體,導致線粒體DNA損傷、功能障礙以及結構完整性被破壞。
當通過電子傳遞鏈(ETC)的電子流受到抑制時,受損的線粒體進一步導致ROS升高,從而增加超氧化物的產生。
線粒體功能障礙損害腸道屏障,改善線粒體功能有助于腸道屏障的恢復:
①mtROS表達上升會激活NLRP3炎癥小體,促進IL-1β和IL-18等炎癥細胞因子的成熟和分泌,加劇炎癥反應。一項臨床前研究表明,IL-18通過阻止結腸中的杯狀細胞成熟和分化,放大了結腸炎期間的腸道損傷并導致屏障功能障礙。
②具有相同核基因組但具有增強粘膜OxPHOS和ATP水平的mtDNA多態性的共生小鼠表現出對葡聚糖硫酸鈉(DSS)誘導的結腸炎的保護作用;線粒體生物發生的主要調節因子(PGC1A)的激活可以恢復線粒體完整性和腸道屏障功能,并有助于減輕DSS結腸炎小鼠的腸道炎癥;此外,促炎細胞因子TNF和IL-1β(在IBD中上調)靶向線粒體以抑制ETC復合物I并增加培養細胞系中mtROS的產生,抗TNF療法顯示出對腸道和其他發炎器官線粒體功能障礙的保護作用。
③除mtROS外,線粒體功能障礙還導致mtDNA 釋放到胞質中或細胞外,充當損傷相關分子模式(DAMP)誘導炎癥信號傳導。氧化的mtDNA可以激活toll樣受體、cGAS-STING信號傳導和NLRP3炎癥小體,以增加原代細胞中的炎性細胞因子。多項研究表明IBD患者循環中mtDNA增加。mtDNA釋放的機制尚未完全闡明,但臨床前研究表明VDAC1參與線粒體外膜的寡聚化和孔形成。用VDAC1寡聚化抑制劑VBIT-4和VBIT-12治療的小鼠免受DSS誘導的結腸炎、相關mtDNA 釋放和NRLP3炎癥小體激活的影響。
這些結果表明,靶向VDAC1和mtDNA 釋放可能是IBD的有益治療策略。
線粒體功能障礙與NAD缺乏之間的聯系:
NAD是參與許多信號通路和線粒體代謝的重要中間體。NADH是NAD的還原形式,通過向ETC復合物I提供電子被氧化為NAD,從而驅動OxPHOS。NAD濃度水平降低可導致SIRT1和SIRT3的活性降低,它們是線粒體穩態的調節因子,包括代謝(OxPHOS、乙酰輔酶A和FAO的產生)、生物發生和抗氧化反應。
在小鼠實驗性結腸炎期間,IECs中NAD濃度水平降低,導致SIRT1活性降低無法激活PGC1A來抑制線粒體生物發生。使用煙酰胺核苷(一種NAD前體)靶向恢復NAD水平的治療方法被證明可以抑制小鼠的實驗性結腸炎并恢復依賴于IEC PGC1A激活的線粒體功能。
健康和疾病狀態下腸道微生物群對線粒體的調控作用:健康狀態下,腸道菌群代謝產生短鏈脂肪酸(SCFAs),促進IEC的氧化磷酸化,維持腸道微環境的厭氧狀態,形成有益的反饋循環。
IBD病理狀態下,腸道菌群的組成改變,SCFAs代謝減少,使IEC轉向更依賴糖酵解的代謝,導致IEC線粒體功能紊亂,進而促進致病菌的生長和炎癥的發展。
線粒體質量控制的改變:線粒體質量控制機制,包括線粒體自噬、線粒體生物合成、分裂與融合,對于維持IEC的線粒體健康和功能至關重要。在IBD中,這些質量控制機制可能發生紊亂,導致線粒體功能障礙,進而影響IEC的穩態和炎癥反應。例如,新診斷的潰瘍性結腸炎患者表現出PGC1A(線粒體生物發生的主要調節因子)和調節ATP產生的基因抑制。自噬受損的小鼠模型表現出受損線粒體的積累和隱窩細胞死亡。
三、上皮細胞線粒體在結直腸癌(CRC)發展中的作用
CRC代謝:CRC的代謝表型是異質性和動態的,一些腫瘤細胞表現出糖酵解代謝偏好,也有一些細胞依賴線粒體氧化磷酸化來滿足能量和生物合成需求。
結直腸癌早期線粒體代謝的作用:在CRC的早期階段,ISCs中線粒體丙酮酸載體(MPC)的下調可阻止丙酮酸進入線粒體,并通過氧化磷酸化(OxPHOS)抑制葡萄糖代謝。這一過程導致有氧糖酵解和乳酸形成上調。線粒體代謝通過脂肪酸和谷氨酰胺向脂肪酸氧化(FAO)轉變。此外,脂肪飲食或肥胖觸發了ISCs脂肪酸氧化,并在驅動腫瘤發生的初始階段中起著主導作用。
結直腸癌晚期線粒體代謝的作用:高結直腸癌晚期的癌細胞根據營養物質的可利用性和腫瘤微環境,通過線粒體代謝葡萄糖、脂肪酸和谷氨酰胺。當線粒體損傷時(缺氧或膜電位喪失),會通過激活WNT信號通路刺激線粒體生物發生,增加線粒體數量,促進腫瘤進展。WNT信號也被線粒體FAO激活。NOTCH通路通過線粒體融合蛋白和Bcl-xL激活促生存信號通路,這些線粒體蛋白致力于維持線粒體的生物能學和功能,進而使CRC細胞存活和腫瘤進展。
CRC中的線粒體自噬:線粒體自噬在結直腸癌中的作用仍然存在爭議。有研究表明線粒體自噬可以去除受損的線粒體,調節線粒體穩態并激活經典致癌途徑促進CRC。但也有研究表明增強線粒體自噬可以激活IEC的適應性免疫反應,從而抑制腫瘤細胞的形成和發展。基于這些觀察結果,考慮線粒體自噬的沖突作用可能歸因于其CRC模型的不同。
四、靶向線粒體治療IBD和CRC
靶向線粒體治療IBD和CRC的潛力:
對于IBD,可能受益于線粒體靶向治療的患者可能包括那些攜帶與線粒體功能或自噬受損(影響線粒體自噬)相關的IBD風險等位基因的患者、循環mtDNA水平高的患者、線粒體誘導的上皮屏障功能障礙或潰瘍的患者或粘膜線粒體功能障礙相關的微生物群生態失調轉化的患者。對于CRC,線粒體靶向療法提供了一種改變代謝和ATP產生的方法,而ATP是腫瘤生長和進展的核心。
IBD中的線粒體靶向治療:
IBD的治療包括線粒體ROS(mtROS)抑制劑(如MitoQ)、NLRP3炎性小體抑制劑(如GSK1070806、非諾貝特和阿托伐他汀)、PGC-1α激活劑(如羅格列酮)、短鏈脂肪酸等。這些治療旨在增強線粒體功能、抑制炎癥和促進黏膜修復。
CRC中的線粒體靶向治療:CRC的治療包括抑制線粒體呼吸的藥物(如二甲雙胍、mito-CP、5-ASA、度維利塞和青霉素)、ROS激動劑(如度維利塞和條葉薊素)以及caspase介導的凋亡誘導劑(如5-ASA、阿司匹林和青霉素)等。這些治療旨在通過影響線粒體功能和代謝來抑制腫瘤生長和轉移。
五、線粒體功能障礙與IBD和CRC的因果關系
IBD和CRC導致線粒體功能障礙:在IBD中,炎癥介質、ROS和微生物產物可直接損害線粒體,表明線粒體健康受損是活動性炎癥的下游結果。在這種情況下,抑制炎癥反過來會挽救線粒體健康,但未來需要詳細的研究來證明這一點。在CRC中,腫瘤微環境的變化和代謝重編程可能導致線粒體功能的適應性變化,促進腫瘤細胞的增殖和存活。
線粒體功能障礙引起IBD和CRC:對于IBD來說,在具有線粒體相關基因突變的患者中,線粒體的改變是驅動疾病的起始事件。具有線粒體功能基因突變的小鼠模型,表現出自發性腸道炎癥,并表明線粒體功能障礙與其他損傷(微生物群、環境觸發因素和持續性線粒體損傷)相結合時可能是疾病的原因。對于CRC來說,腫瘤轉化前結腸ISC中的mtDNA突變以及線粒體代謝改變驅動CRC的起始。
研究總結
線粒體代謝和信號傳導的改變與胃腸道疾病有關,包括IBD和CRC。上皮線粒體是ROS氧化損傷、促炎細胞因子和影響線粒體健康、代謝和IBD致病信號傳導的微生物代謝物的下游靶標,包括細胞質和線粒體ROS 升高、NLRP3激活和mtDNA釋放。它們會聚集以損害屏障功能,誘導IEC死亡和微生物群失調轉變。
就CRC而言,線粒體功能障礙與在慢性損傷存在下啟動腫瘤發生的細胞類型改變有關。在結直腸癌的晚期,線粒體代謝會促進癌癥的生長。隨著線粒體靶向治療在這些疾病中的測試,人們可以想象一種更加個性化的方法,用于基于基因突變、線粒體代謝或應激生物標志物的特定亞型患者,作為當前治療的雙重方法。
課題標書服務
時間緊張:如果拿不準標書質量,或者沒有任何標書撰寫經驗,不妨試試我們的課題標書服務
沒基礎沒經驗,標書寫不出來?
真實實驗室提供預實驗協助:隨著課題晉升比重的不斷加大,立項標準也水漲船高。以前中不中只看標書,現在評審專家對是否有預實驗也很看重!
對于省市級課題,有預實驗加持中標幾率明顯更高!
交付完整標書:立項依據、研究方案、經費預算等,無需做修改,可直接上傳申報系統。還有清晰研究思路文檔,無懼單位審查。
沒時間沒精力,還沒申報就開始泄氣?
NO!你離中標,只差一個免費的掃碼咨詢


 長按圖片保存/分享
長按圖片保存/分享
147









 在線咨詢
在線咨詢

