
Advanced Science“新賽道”!腸道菌群搭檔“天然產物”想不火都難!浙江大學團隊這波思路真的很行!
瀏覽:93
發表時間:2025-08-14
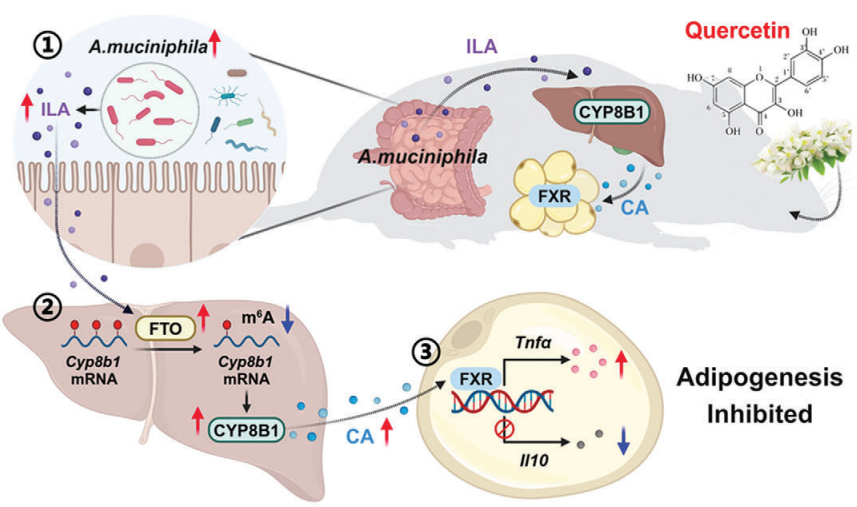
今天分享的這篇文章是2025年1月31日由浙江大學王新霞團隊發表在Advanced Science上題為:Quercetin-Driven Akkermansia Muciniphila Alleviates Obesity by Modulating Bile Acid Metabolism via an ILA/m6A/CYP8B1 Signaling的研究論文,研究提出了一個新的代謝調控軸:ILA/m6A/CYP8B1/CA,揭示了微生物代謝產物ILA通過m6A修飾調控CYP8B1的表達,進而影響膽汁酸代謝,最終抑制脂肪積累。
綜合運用了16S rDNA測序、非靶向代謝組學、細胞實驗、基因沉默、m6A修飾分析等多種技術手段,提出了一個全新的代謝調控軸,即槲皮素(Quercetin)驅動的腸道菌(Akkermansia muciniphila)通過ILA/m6A/CYP8B1信號調節膽汁酸代謝來緩解肥胖。從腸道菌群切入研究天然產物機制,既迎合了國自然的“偏向”,同時又很創新,想做課題設計的朋友完全可以參考這篇文章的思路,利用“組學”研究互作機制,一舉拿下國自然!文章&項目雙贏!想復現這種思路或者定制更多創新性思路歡迎聯系大仲!

研究背景
全球健康正面臨肥胖及其相關并發癥日益增長的挑戰。槲皮素作為一種重要的天然黃酮類化合物,具有抗氧化、抗肥胖等多種生物活性,但其作用機制尚不清楚。近年來,研究發現腸道微生物群在調節宿主代謝過程中發揮重要作用,而槲皮素可能通過與腸道微生物相互作用來發揮其健康益處。
研究主要結果
1.槲皮素可以改善HFD誘導的肥胖癥和相關代謝失調
為了研究槲皮素對體內代謝和脂肪積累的生理影響,雄性C57 BL/6 J接受正常食物飲食(NCD)、補充有NCD+Que、HFD或補充有HFD+Que持續10周(圖1)。總之,最終結果表明槲皮素提供了對HFD誘導的肥胖和相關代謝功能障礙的保護。最終證實了A.mucinophila有利于代謝的體內平衡,并且與肥胖特征負相關。
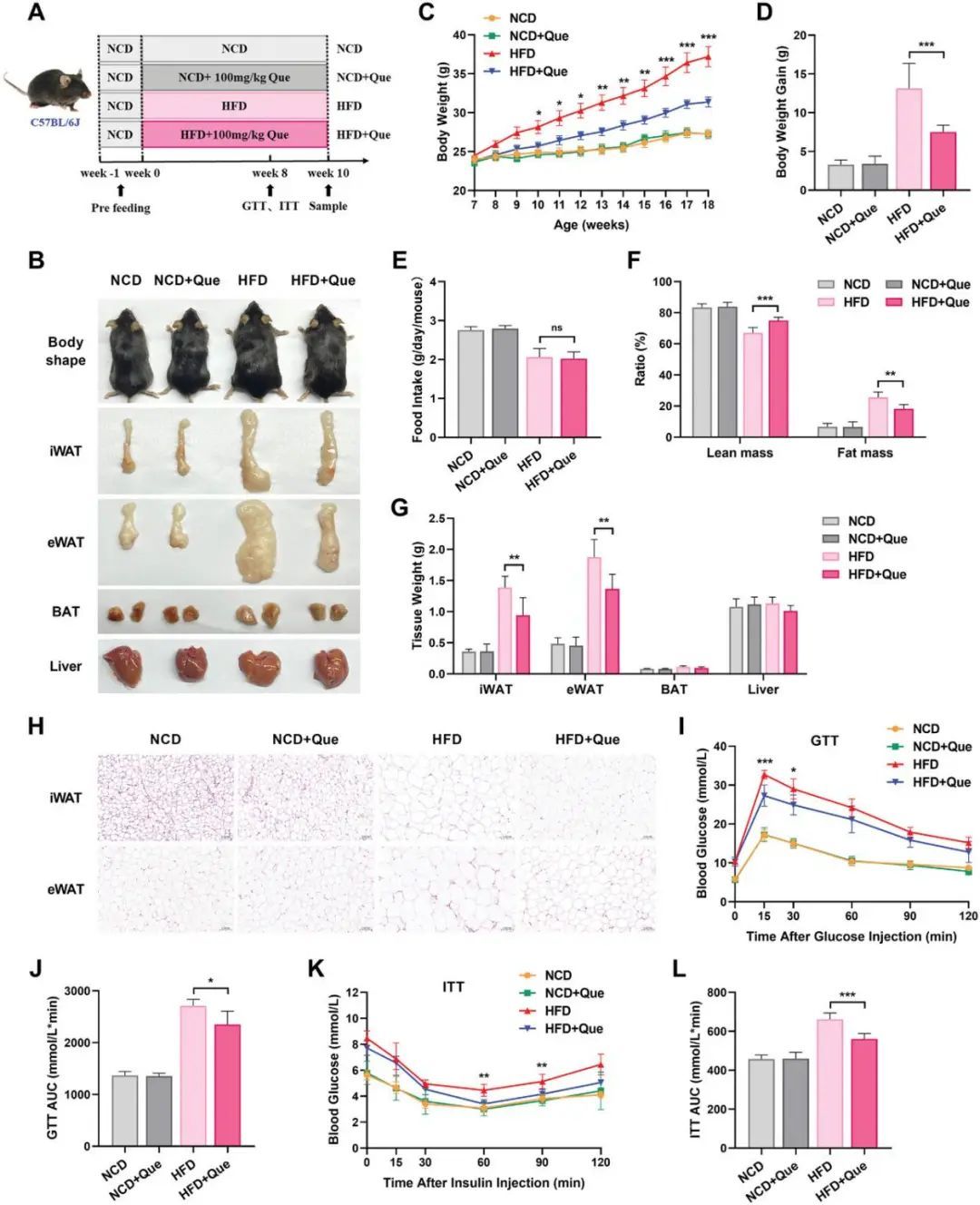
圖1.槲皮素改善飲食誘導的肥胖癥和相關的代謝紊亂。A)對C57 BL/6 J施用槲皮素的實驗設計的示意圖。B)體型、iWAT、eWAT、BAT和肝臟的代表性照片。C)體重的動態變化。D)研究結束時的相對體重增加。E)攝食量。F)小鼠的瘦肉和脂肪組織的身體組成參數。G)研究結束時的iWAT、eWAT和BAT重量。H)iWAT和eWAT的代表性H&E染色。I,J)腹膜內注射葡萄糖進行GTT后的血糖水平。根據GTT結果(I)計算AUC。K,L)腹腔注射胰島素進行胰島素耐受試驗后小鼠的ITT。根據ITT結果(L)計算AUC。
2.槲皮素重塑了微生物群的整體結構,特別升高了粘麥那霉素的豐度
值得注意的是,A.mucinophila一種有前景的益生菌在HFD+Que中富集(圖2)。由于在基礎飼料條件下給予槲皮素,其相對豐度也較高。此外,斯皮爾曼的相關分析表明,A.mucinophila是唯一與代謝參數顯著負相關的微生物,如體重增加、脂肪質量百分比和iWAT重量,最終證實了A.mucinophila有利于代謝的體內平衡,并且與肥胖特征負相關。
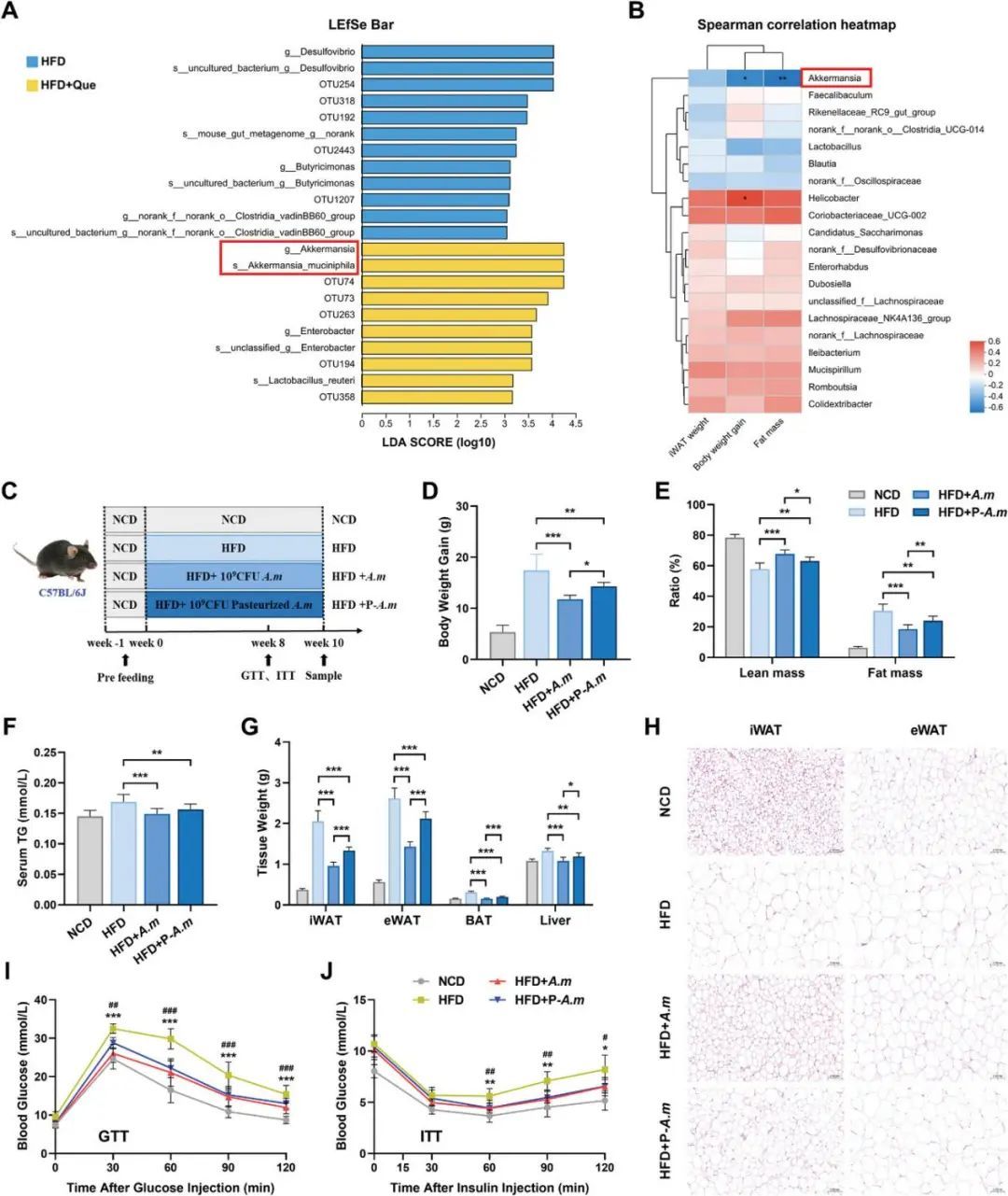
圖2.槲皮素重組了微生物群落A)LEfSe分析鑒定了HFD和HFD+Que組之間細菌豐度。B)糞便細菌豐度與所選代謝參數之間的斯皮爾曼相關系數。C)施用A的實驗設計示意圖。D)研究結束時小鼠的相對體重增加。E)小鼠的瘦肉和脂肪組織的體成分參數。F)小鼠中總TG的血清水平。G)研究結束時的iWAT、eWAT和BAT重量。H)小鼠iWAT和eWAT的代表性H&E染色。
3.A. muciniphila增加血清CA水平,從而通過FXR信號抑制脂質積累
為了鑒定可以調節脂質沉積的潛在代謝物,對從HFD和HFD+A收集的血清樣品進行非靶向代謝組學分析。PLS-DA表明,20種代謝產物的集合表現出顯著的變化:在HFD+A中,19種代謝產物明顯上調,而1種代謝產物顯著下調(圖3),總之,作者的數據揭示了A.mucinophila對BA代謝有調節作用。增加循環CA水平抑制脂質積累的方式依賴于BAs受體FXR。
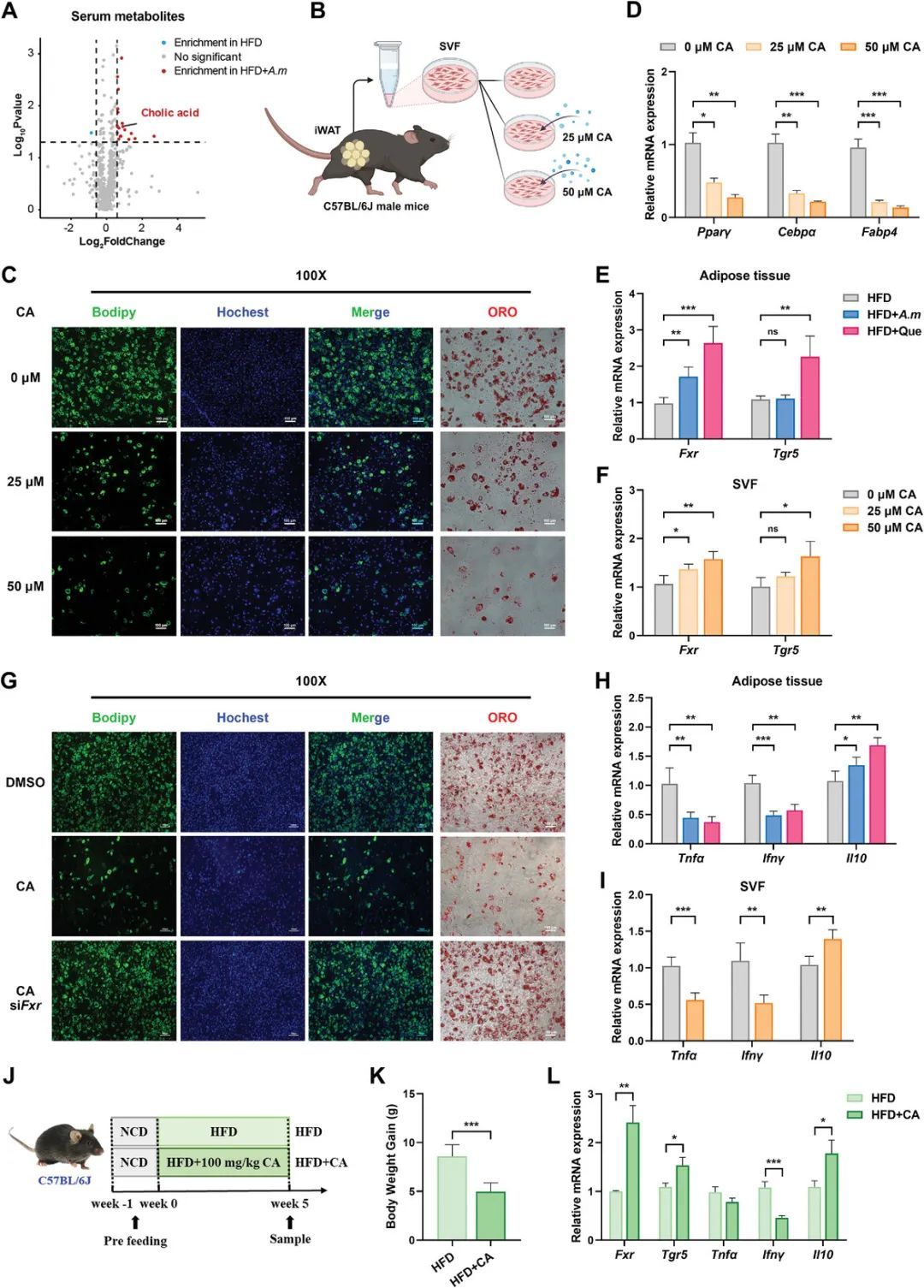
圖3.CA通過FXR信號傳導提供抗肥胖的保護。A)火山圖顯示了A.mucinophila液菌定居。B)體外細胞實驗示意圖。C)SVF細胞的Bodipy和ORO染色。D)SVF細胞中脂肪形成相關標記基因的mRNA表達水平(n = 4)。主要BAs受體(Fxr和Tgr 5)在iWAT(E)和SVF細胞中的mRNA表達水平
4.A. muciniphila代謝物以m6A依賴性方式增強CYP8B1的表達,從而上調CA水平
為了進一步鑒定A.mucinophila也影響體外CA水平,作者加入了A.mucinophila培養上清(A.m-Sup)加入AML 12細胞培養基中,空白腦心灌注(BHI)培養基上清液(BHI-Sup)作為對照(圖4)。與體內觀察結果一致,最終作者發現A.mucinophila從表觀遺傳學的角度,嗜粘液菌調節BA代謝,從而減輕宿主肥胖。
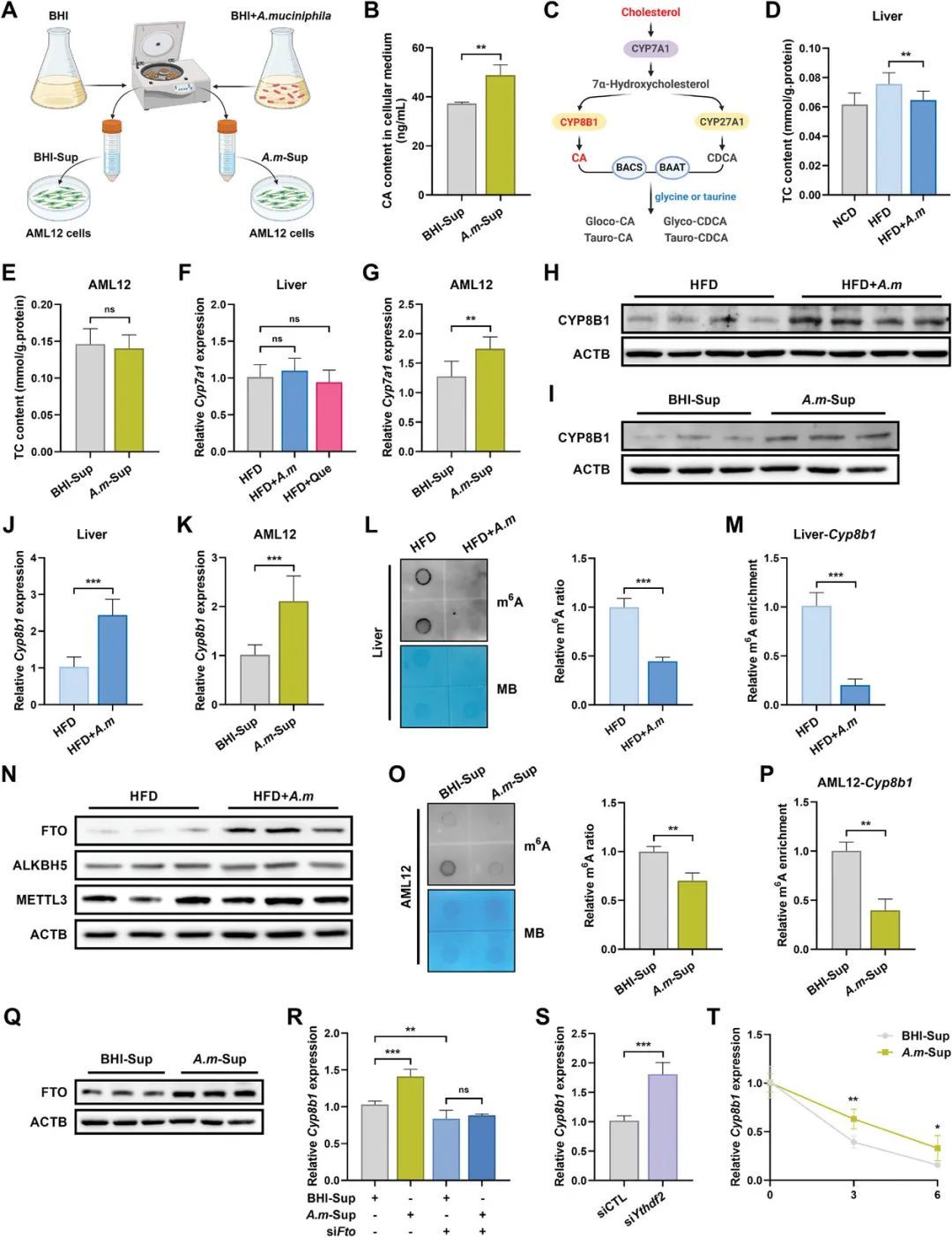
圖4 A.mucinophila代謝物以m6 A依賴性方式增強CYP 8B 1表達,以產生更多CA。A)收集A.mucinophila以空白BHI上清作為對照。B)AML 12細胞培養基中的CA濃度。C)BA代謝途徑的示意圖。D)小鼠肝臟的TC含量。E)用BHI-Sup或A.m-Sup組。F,G)肝(F)和AML 12細胞(G)中Cyp 7a 1的mRNA表達水平。H,I)肝臟(H)和AML 12細胞(I)中CYP 8B 1的蛋白表達水平。肝(J)和AML 12細胞中Cyp 8b 1的mRNA表達水平
5.代謝產物ILA負責增加m6A介導的CYP8B1表達
隨后,作者檢查了A.mucinophila通過非靶向代謝物組學分析鑒定了A.mucinophila嗜粘液菌屬(圖5)。
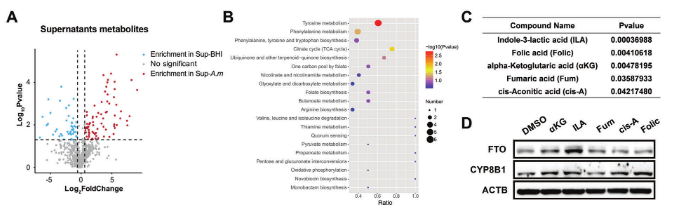
圖5.代謝產物ILA可導致m6A介導的CYP8B1水平上調。A)顯示空白BHI上清液和A.mucinophila培養上清液。B)(A)中描述的差異表達的代謝物的KEGG富集分析。C)篩選出的A.mucinophila嗜粘液菌屬。
文章小結
在機制上,作者證明了A.muciniphila及其代謝產物ILA通過增加FTO-m6 A-YTHDF 2信號傳導中CYP 8B 1的表達來調節CA代謝。CYP 8B 1的上調表達促進膽固醇向CA的轉化,進而通過激活脂肪組織中的法尼醇X受體(FXR)顯著抑制脂質蓄積。“腸道菌群”的熱度近年來一直居高不下,豐富的腸道菌群和組學分析實在太適配了!
如有需要,請聯系我們~
主營項目
1. 動物實驗
動物飼養、疾病造模、行為學檢測、心功能、無創血壓、血常規、全自動生化檢測等
2. 細胞實驗
CCK8/MTT、原代細胞分離、流式細胞實驗、細胞劃痕、侵襲、遷移、EDU染色、轉染、穩定株
3. 分子生物學
PCR檢測、熒光定量PCR、絕對定量PCR、端粒酶長度、pull down、雙熒光素酶、SSR、SNP檢測等
4. 蛋白實驗
WB、Co-IP、酵母雙雜
5. 病理實驗
HE染色、免疫組學、電鏡
6. 生理生化實驗
肝腎功能、抗氧化、免疫反應等生理免疫指標;動植物營養指標、微量元素、重金屬、酶活等。
7. 多組學實驗
基因組、轉錄調控、蛋白組、代謝組、微生物多樣性、宏基因組、生信分析
8. 整體課題實驗
方案設計、整體實驗交付、標書寫作、論文潤色、協助投稿
聯系我們
康旭禾生物提供包括動物實驗、細胞實驗、分子實驗、病理實驗、流式檢測實驗及論文翻譯、潤色、投稿輔助等相關的各項服務。
聯系方式:15579126092
公司官網:http://consurebio.com/
公司地址:江西省南昌市南昌縣小藍VR產業基地D座2樓


 長按圖片保存/分享
長按圖片保存/分享
93









 在線咨詢
在線咨詢

