
細胞死亡沒啥可研究的了?哈爾濱醫科大學教你整出新花樣:細胞焦亡+炎癥小體+乙酰化+類器官,這“逆天”思路審稿人看了都點贊!
瀏覽:27
發表時間:2025-08-26
親愛的小伙伴們,你們最近科研進展的還順利嗎?最近看到一個新聞非常氣憤,廣東工業大學有兩研究生,他們暑假留校參與課題科研工作,但因為午休時間打游戲看視頻娛樂被嚴厲地處罰。真的是沒有天理了啊,午休時間都不能讓人休息。還是建議各位小伙伴們要適當的娛樂休息,這樣才能更好地投入科研事業!接下來給大家推薦一篇思路絕佳的文章,它將細胞焦亡、炎癥小體、乙酰化和類器官結合在一起,快來看一下吧~
1.多種方法進行驗證:研究使用各種技術評估了用抗腫瘤藥物治療的CRC細胞中的細胞焦亡,包括蛋白質印跡、乳酸脫氫酶釋放試驗和顯微鏡分析。為了揭示調節NLRP3的表觀遺傳機制,使用轉座酶可及染色質測定法和RNA測序評估了染色質變化和NLRP3啟動子組蛋白修飾。染色質免疫沉淀定量聚合酶鏈反應用于研究NLRP3轉錄調控機制。此外,還構建異種移植和患者來源的異種移植模型來驗證藥物組合的效果。
2.具有臨床意義:研究揭示了HDAC2在抑制NLRP3/GSDMD介導的CRC細胞焦亡中起著至關重要的作用,并強調HDAC2是抗腫瘤治療的潛在治療靶點。

題目:抑制HDAC2可促進NLRP3/GSDMD介導的結腸直腸癌細胞焦亡,從而增強抗腫瘤治療的敏感性雜志:Clinical and Translational Medicine影響因子:IF=7.9發表時間:2024年6月研究背景結直腸癌(CRC)占全球癌癥發病率和死亡率的10%左右。大約一半被診斷患有CRC的患者最終會發展為轉移性結直腸癌(mCRC),主要治療方式是化療和靶向治療。目前大量研究表明激活的細胞焦亡可以增強多種腫瘤的抗腫瘤治療效果,但結直腸癌(CRC)中細胞焦亡的具體機制仍不清楚。
研究思路 
研究結果1.CRC中NLRP3沉默抑制了抗腫瘤治療期間GSDMD介導的細胞焦亡免疫組織化學分析顯示,與相應的相鄰正常對照相比,CRC組織中的NLRP3表達顯著降低,而GSDMD表達保持不變(圖1A、B)。mRNA和蛋白質水平顯示,NLRP3表達在原發性CRC組織中降低(圖1C)。同樣,觀察到NLRP3在大多數CRC細胞系中被沉默,而GSDMD則廣泛表達(圖1D)。研究選擇了四種具有差異NLRP3表達的CRC細胞系來測試藥物誘導的細胞焦亡:NLRP3表達相對較高的HCT116和DLD1,以及表達相對較低的SW620和LS174T(圖1D)。
Western blot分析顯示,NLRP3沉默抑制了細胞焦亡途徑的激活:Caspase1、GSDMD cleavage和Pro IL1β/IL-18釋放減少(圖1E)。經過36小時的瑞戈非尼或5-FU處理后,超過30%的NLRP3高表達腫瘤細胞表現出明顯的焦亡形態,包括核固縮、細胞腫脹和膜起泡,而只有約2%的NLRP3低表達細胞表現出類似的形態變化(圖1F)。
通過在流式細胞術分析中進行Caspase-1/PI雙重染色,與NLRP3表達低的細胞相比,使用瑞戈非尼或5-FU在表達高水平NLRP3的細胞中誘導的焦亡百分比(Caspase-1+/PI+)明顯更高(圖1G、H)。NLRP3高表達腫瘤細胞表現出比NLRP3低表達細胞明顯更高的LDH釋放,這表明高水平的NLRP3導致細胞膜損傷增加(圖1I)。綜上所述,這些結果表明,沉默NLRP3會損害CRC細胞的細胞焦亡。
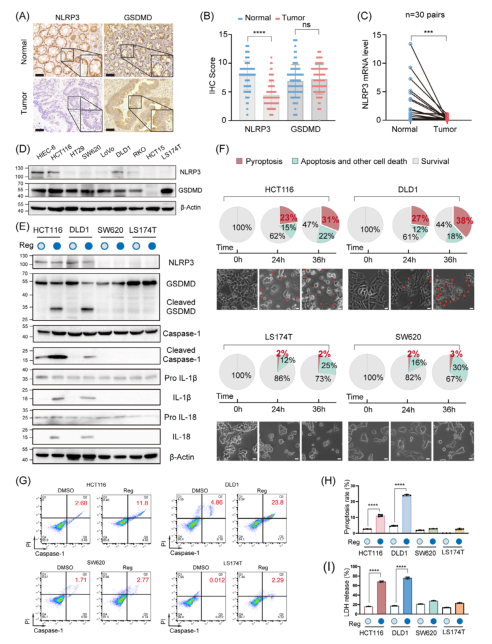
圖1:結直腸癌(CRC)中NLRP3表達的缺失限制了抗腫瘤治療期間gasdermin D(GSDMD)介導的細胞焦亡2.在CRC細胞中補充NLRP3表達可在體內和體外挽救GSDMD介導的細胞焦亡與野生型細胞相比,NLRP3過表達不會影響細胞焦亡標志物GSDMD、Pro IL-1β、Pro IL-18和Caspase-1的裂解,但在使用瑞戈非尼或5-FU等各種化療藥物治療后觀察到顯著增加(圖2A)。
此外,與對照組相比,NLRP3過表達增強了多種藥物誘導的LDH釋放,并降低了CRC細胞的細胞活力(圖2B、C)。使用高分辨率掃描電子顯微鏡分析受損的NLRP3過表達細胞,超微結構膜突起更明顯(圖2D、E)。Caspase-1/PI流式細胞術測定,與對照組相比,NLRP3過表達細胞中的細胞凋亡百分比(Caspase-1+/PI+)顯著增加(圖2F,G)。通過皮下注射NLRP3過表達的SW620細胞,構建異種移腫瘤模型。與對照異種移植相比,在12天的時間內,NLRP3過表達的腫瘤在接受瑞戈非尼或5-FU治療后顯示出腫瘤生長減弱,最終腫瘤負擔減輕(圖2H、I)。
免疫組織化學(IHC)和蛋白質印跡分析表明,與對照腫瘤相比,持續給藥后,腫瘤內細胞焦亡相關標志物(Cleaved caspase-1和Cleaved GSDMD)的水平升高(圖2J)。綜上所述,NLRP3重新表達促進CRC細胞的細胞焦亡。
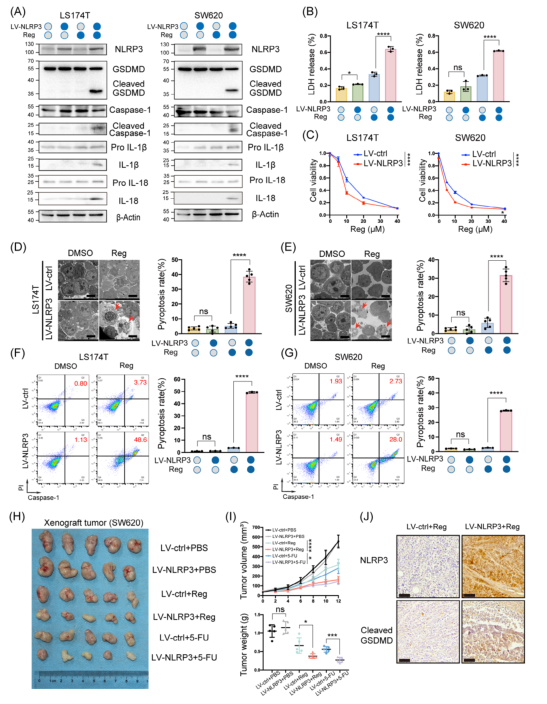
圖2:在結直腸癌(CRC)細胞中補充NLRP3表達可在體內和體外挽救Gasdermin D (GSDMD)介導的細胞焦亡3.HDAC2介導的組蛋白去乙酰化導致CRC中NLRP3的表觀遺傳沉默表觀遺傳藥物的篩選表明SAHA和VPA是CRC細胞中NLRP3的強效誘導劑,可顯著提高轉錄本和蛋白質表達(圖3A-C)。SAHA和VPA劑量依賴性地提高了四種結腸癌細胞系中的NLRP3水平(圖3D、E)。
Spearman相關系數分析揭示了NLRP3與大多數HDAC之間存在負相關性。同時,這些去乙酰化酶的siRNA篩選表明,只有HDAC2敲低才會增加CRC細胞中的NLRP3轉錄(圖3F)。
免疫印跡結果表明,相對于正常鄰近組織,患者來源的CRC組織表現出較高的HDAC2蛋白豐度,這與NLRP3水平呈負相關(圖3G)。此外,CRC細胞系的蛋白質印跡分析證實了HDAC2和NLRP3表達呈反比(圖3H)。
TCGA數據分析顯示,與正常樣本相比,CRC樣本中的HDAC2表達上調(圖3I)。值得注意的是,用選擇性HDAC2抑制劑SCA治療可誘導結腸癌細胞中NLRP3水平的劑量依賴性上調(圖3J)。與非靶向siNC轉染相比,siHDAC2轉染顯著提高了NLRP3的蛋白質水平(圖3K)。這些結果表明,CRC中HDAC2異常高表達導致NLRP3的表觀遺傳沉默。
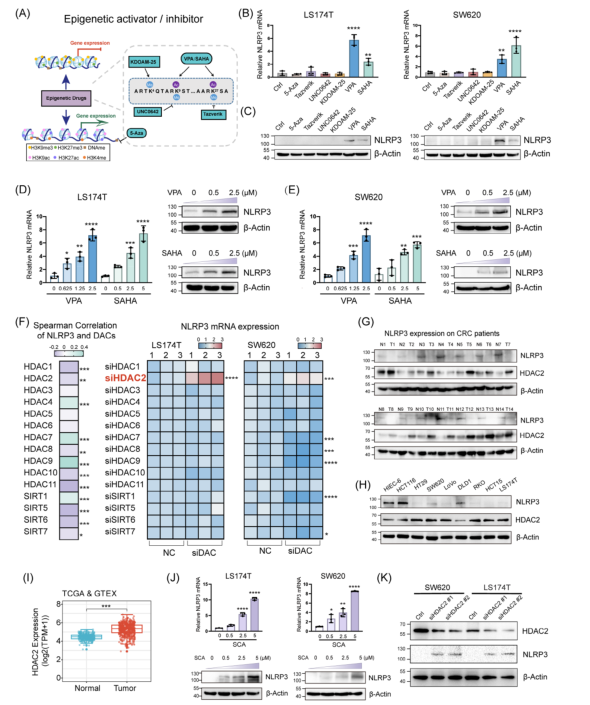
圖3:HDAC2介導的組蛋白去乙酰化導致結直腸癌(CRC)中NLRP3的表觀遺傳沉默4.敲除HDAC2可通過上調NLRP3激活GSDMD介導的細胞焦亡蛋白質印跡分析證實,HDAC2缺失導致GSDMD和IL1β裂解(圖4A)。然而,在HDAC2缺陷細胞中敲低NLRP3會減弱這些蛋白質的裂解(圖4B)。與對照細胞相比,HDAC2 KO細胞中的LDH水平升高,并且也可以通過敲低NLRP3來逆轉這一現象(圖4C、D)。使用具有不同HDAC2表達水平的PDO培養物進行了實驗。暴露于瑞戈非尼后,與具有較高HDAC2表達水平(PDO-1)的類器官相比,具有較低HDAC2表達水平(PDO-2)的類器官表現出更明顯的形態破壞(圖4E)。
光學顯微鏡顯示,約30%-40%的HDAC2 KO結腸癌細胞在藥物治療后表現出焦亡形態(特征性細胞膜膨脹),而野生型細胞僅有3%-6%出現焦亡形態(圖4F)。然而,在HDAC2 KO系中通過siRNA介導敲低NLRP3可顯著降低焦亡細胞比例至10%以下(圖4G)。 研究進行了Caspase-1和PI雙染。結果顯示,在HDAC2 KO后,瑞戈非尼或5-FU誘導的細胞焦亡水平增加,而在NLRP3敲低(siNLRP3)后,細胞焦亡水平降低(圖4H、I)。總之,結果確定了NLRP3是HDAC2的一個重要功能靶點,并證實HDAC2通過調節NLRP3水平來控制結直腸癌的藥理學細胞焦亡。
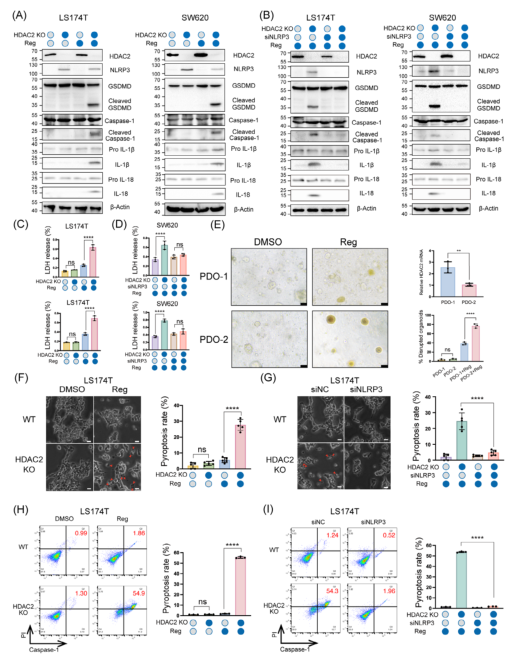
圖4:敲除HDAC2可通過上調NLRP3來激活gasdermin D(GSDMD)介導的細胞焦亡5.HDAC2通過抑制染色質可及性來阻斷p-P65對NLRP3的轉錄作用熱圖顯示,HDAC2沉默并未顯著改變SW620細胞中的整體染色質可及性(圖5A)。對按HDAC2 KO后染色質可及性變化排序的基因進行GSEA。結果表明,焦亡途徑顯著富集,排名第一(圖5B)。染色質可及性變化的可視化顯示開放染色質結構增強,特別是在NLRP3啟動子處,而其他焦亡基因GSDMD、Caspase-1和PYCARD的調控區沒有類似的影響(圖5C)。之前的研究表明,瑞格非尼通過抑制GSK3β(Ser9)自磷酸化而顯著增加p-P65(Ser536)的激活(圖5D)。在檢查NLRP3啟動子的DNA序列后,確定了轉錄因子P65的假定結合位點,該位點位于NLRP3轉錄起始位點上游?1086至?1077bp(GGGAATTTCC)處(5E)。隨后的ChIP測定表明,在HDAC2 KO或用HDAC2特異性抑制劑SCA治療后,轉錄因子pP65與NLRP3啟動子區域的結合增強(圖5F)。
Western blot分析顯示,用瑞戈非尼處理的HDAC2 KO細胞中NLRP3水平顯著增加(圖5G)。這些結果表明,HDAC2 KO提高了NLRP3啟動子處的染色質可及性,從而允許在藥物誘導條件下募集更多的p-P65,促進NLRP3轉錄激活。
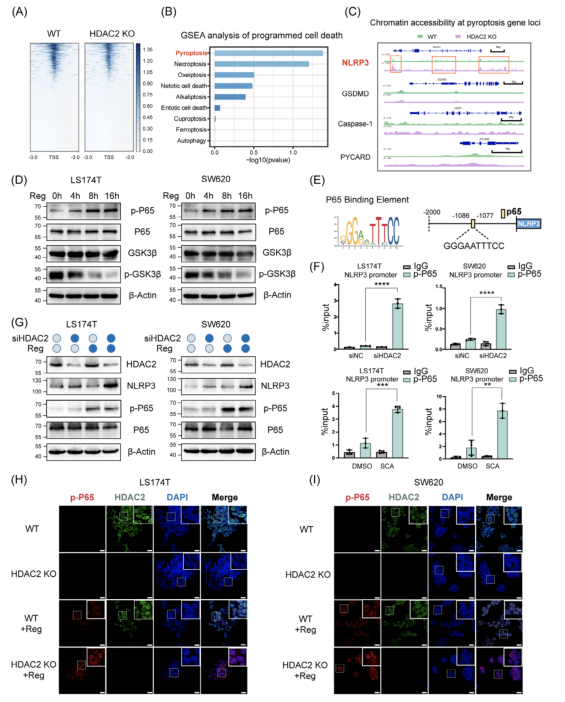
圖5:HDAC2通過抑制染色質可及性來阻斷p-P65對NLRP3的轉錄作用6.抑制HDAC2可促進H3K27ac-BRD4-p-P65復合物的形成,從而激活NLRP3轉錄通過分析ChIP-seq數據集,與THP-1細胞和結腸隱窩細胞相比,CRC細胞中NLRP3啟動子區域內的H3K27乙酰化水平明顯較低(圖6A)。ChIP表明,在HDAC2缺失后,NLRP3基因啟動子處的H3K27ac增加,但H3K9ac沒有增加(圖6B)。
Western blot分析表明,與對照相比,HDAC2 KO細胞中的H3K27ac水平增加,NLRP3表達也相應增加(圖6C)。
熒光顯微鏡分析顯示,與野生型對照相比,瑞戈非尼治療后,HDAC2 KO細胞中的核H3K27乙酰化增加,并且HDAC2 KO細胞中的p-P65核募集增強(圖6D、E)。在細胞中進行免疫共沉淀實驗,觀察到內源性BRD4與P65和H3K27ac形成NLRP3復合物,在HDAC2 KO時該復合物得到增強(圖6F)。此外,使用p-P65抗體的ChIP表明,在HDAC2 KO CRC細胞中,BRD4 siRNA處理抑制后,NLRP3啟動子上的p-P65占有率降低(圖6G)。結果表明,HDAC2缺失增加了H3K27ac,促進了H3K27ac-BRD4-p-P65復合物的形成,從而招募更多的p-P65并驅動NLRP3轉錄激活。
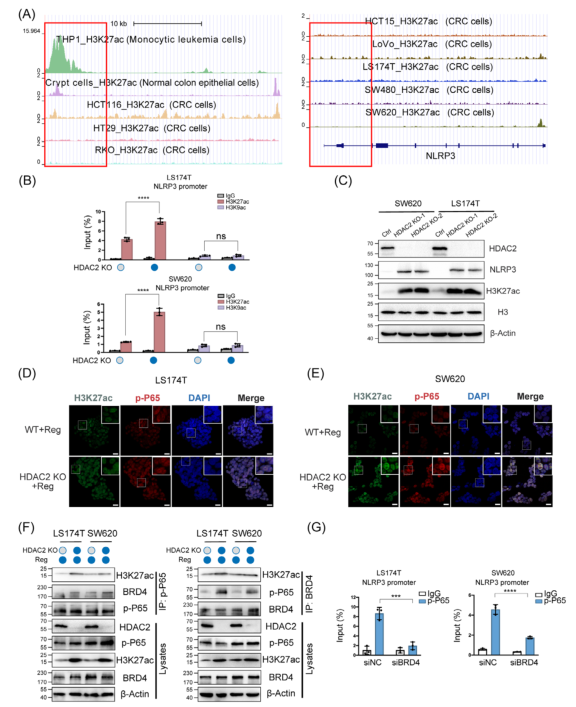
圖6:抑制HDAC2可促進H3K27ac-BRD4-p-P65復合物的形成,從而激活NLRP3轉錄7.HDAC2與H3K27ac/p-P65/NLRP3相關,可預測預后并代表CRC的一個有希望的靶點研究構建CRC PDX 模型,使用蛋白質印跡法分析腫瘤裂解物顯示,聯合治療組的Cleaved GSDMD升高,表明細胞焦亡,但兩種PDX模型的單藥組均未升高(圖7A、B)。與對照組相比,瑞戈非尼加SCA組的腫瘤大小顯著減小。然而,瑞戈非尼和SCA單獨使用均未在體內顯著抑制腫瘤生長(圖7C、D)。在BP0036模型中,經過相同藥物劑量治療12天后,瑞戈非尼加SCA組的腫瘤生長抑制率明顯高于單獨使用瑞戈非尼治療組(圖7E)。在SW620結腸癌異種移植中也得到驗證,聯合治療比單一治療具有更佳的腫瘤抑制效果(圖7F-H)。通過免疫組織化學染色分析了82例CRC患者標本中HDAC2、NLRP3、H3K27ac和pP65的表達水平,觀察到HDAC2的表達與p-P65、H3K27ac和NLRP3的水平呈負相關(圖7I)。Kaplan-Meier生存分析表明,HDAC2表達高的患者總體生存期較短(圖7J)。
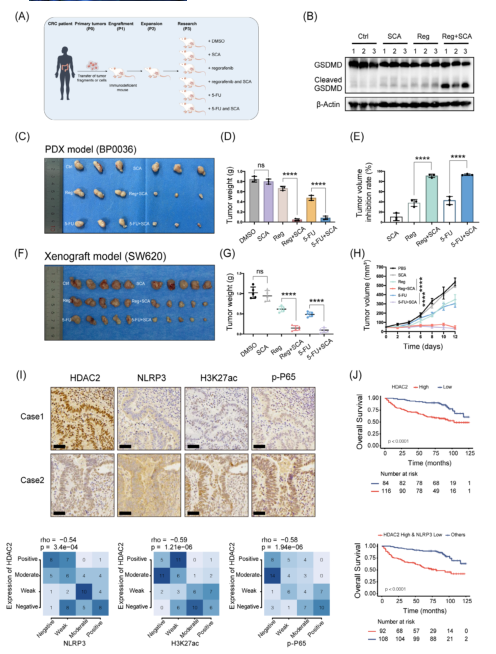
圖7:HDAC2與H3K27ac/p-P65/NLRP3相關,可預測預后并代表結直腸癌(CRC)的一個有希望的靶點
文章小結本研究表明CRC中HDAC2的過度表達導致NLRP3的表觀遺傳抑制,阻礙藥物治療引起的細胞焦亡。抑制HDAC2有助于形成H3K27ac-BRD4-p-P65復合物,從而促進NLRP3轉錄。這篇文章值得細細品味,除了“細胞焦亡”和“炎癥小體”國自然熱點,還有“乙酰化”和“類器官”,學會這篇文章的研究思路,分分鐘中標~
主營項目
1. 動物實驗
動物飼養、疾病造模、行為學檢測、心功能、無創血壓、血常規、全自動生化檢測等
2. 細胞實驗
CCK8/MTT、原代細胞分離、流式細胞實驗、細胞劃痕、侵襲、遷移、EDU染色、轉染、穩定株
3. 分子生物學
PCR檢測、熒光定量PCR、絕對定量PCR、端粒酶長度、pull down、雙熒光素酶、SSR、SNP檢測等
4. 蛋白實驗
WB、Co-IP、酵母雙雜
5. 病理實驗
HE染色、免疫組學、電鏡
6. 生理生化實驗
肝腎功能、抗氧化、免疫反應等生理免疫指標;動植物營養指標、微量元素、重金屬、酶活等。
7. 多組學實驗
基因組、轉錄調控、蛋白組、代謝組、微生物多樣性、宏基因組、生信分析
8. 整體課題實驗
方案設計、整體實驗交付、標書寫作、論文潤色、協助投稿
聯系我們
康旭禾生物提供包括動物實驗、細胞實驗、分子實驗、病理實驗、流式檢測實驗及論文翻譯、潤色、投稿輔助等相關的各項服務。
聯系方式:15579126092
公司官網:http://consurebio.com/
公司地址:江西省南昌市南昌縣小藍VR產業基地D座2樓


 長按圖片保存/分享
長按圖片保存/分享
27









 在線咨詢
在線咨詢

